![[거대분자] 3.4 프로테오글리칸(proteoglycan) & 당단백질(glycoprotein) 차이](https://i.ytimg.com/vi/sC49D77JITs/hqdefault.jpg)
콘텐츠
-
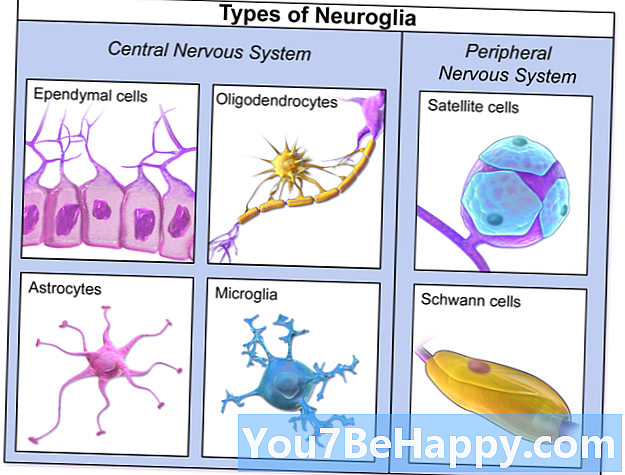
프로테오글리칸
프로테오글리칸은 크게 글리코 실화 된 단백질이다. 기본 프로테오글리칸 단위는 하나 이상의 공유 적으로 부착 된 글리코 사 미노 글리 칸 (GAG) 쇄를 갖는 "코어 단백질"로 구성된다. 부착 지점은 글리코 사 미노 글리 칸이 사당 류 브릿지 (예를 들어, 콘드로이틴 설페이트 -GlcA-Gal-Gal-Xyl-PROTEIN)를 통해 연결된 세린 (Ser) 잔기이다. Ser 잔기는 일반적으로 서열 -Ser-Gly-X-Gly- (여기서 X는 임의의 아미노산 잔기이지만 프롤린 일 수 있음)에 있지만,이 서열을 갖는 모든 단백질이 부착 된 글리코 사 미노 글리 칸을 갖는 것은 아니다. 사슬은 길고 선형 탄수화물 중합체이며, 황산염 및 우론 산기의 발생으로 인해 생리 학적 조건 하에서 음으로 하전된다. 프로테오글리칸은 결합 조직에서 발생합니다.
-
당 단백질
당 단백질은 아미노산 측쇄에 공유 적으로 부착 된 올리고당 사슬 (글리 칸)을 함유하는 단백질이다. 탄수화물은 공 번역 또는 번역 후 변형으로 단백질에 부착된다. 이 과정을 글리코 실화라고합니다. 분비 된 세포 외 단백질은 종종 글리코 실화된다. 세포 외로 연장되는 세그먼트를 갖는 단백질에서, 세포 외 세그먼트는 종종 글리코 실화된다. 당 단백질은 종종 세포-상호 작용에 중요한 역할을하는 중요한 통합 막 단백질입니다. 분비 시스템의 소포체-기반 글리코 실화를 가역적 시토 졸 핵-글리코 실화와 구별하는 것이 중요하다. 세포질 및 핵의 당 단백질은 인산화에 역수로 간주되는 단일 GlcNAc 잔기의 가역적 첨가를 통해 변형 될 수 있으며, 이들의 기능은 인산화-기반 신호 전달을 제어하는 추가 조절 메커니즘 일 가능성이있다. 대조적으로, 고전적인 분비 글리코 실화는 구조적으로 필수적 일 수있다. 예를 들어, 아스파라긴-연결된, 즉 N- 연결된 글리코 실화의 억제는 적절한 당 단백질 폴딩을 방지 할 수 있고 완전 억제는 개별 세포에 독성이 될 수있다. 대조적으로, 소포체와 골지 장치에서 발생하는 글리 칸 가공의 교란 (글리 칸으로의 효소 제거 / 탄수화물 잔류 물의 첨가)은 단리 된 세포에 필수적이며 (글리코 시드 억제제에 의한 생존 증거) 인간으로 이어질 수있다 질병 (선천성 글리코 실화 장애) 및 동물 모델에서 치명적일 수있다. 따라서, 글리 칸의 미세 가공은 세포 밀매와 같은 내인성 기능에 중요하지만, 이는 숙주-병원체 상호 작용에서의 이의 역할에 부차적 일 가능성이있다. 이 후자의 효과의 유명한 예는 ABO 혈액형 시스템입니다.
프로테오글리칸 (명사)
복수의 프로테오글리칸
당 단백질 (명사)
공유 결합 탄수화물을 가진 단백질.
당 단백질 (명사)
폴리펩티드 쇄에 탄수화물 그룹이 부착 된 임의의 부류의 단백질.
당 단백질 (명사)
탄수화물 성분을 갖는 공액 단백질